Ответы и авторские решения на все задания для 7 8 9 10 и 11 класса онлайн олимпиада по химии 17 октября 2025 школьный этап ВСОШ официальной всероссийской олимпиады школьников Москвы всего в олимпиаде 22 заданий от проекта СтоБалловв приступить к прохождению не позднее 19:00 17 октября 2025 года.
Олимпиада по химии ответы 7-8 класс школьный этап 2025
Задание 1. Пламя становится светящимся из-за образующихся в нем раскаленных твердых частиц. Если образующихся частиц слишком много, то они не успевают нагреться в пламени до белого каления, такое пламя коптит. Определите, какие из веществ при сгорании на открытом воздухе дают светящееся или коптящее пламя.
бензин
сера
метан
магний
фосфор
водород
Ответ: сера, метан, магний, фосфор, водород, бензин
Задание 2. На планете Плюк в соседней галактике Периодическая система такая же, как на Земле, но атомная единица массы у них ровно в 3 раза больше.
Чему равна относительная молекулярная масса воды на Плюке?
Ответ: 18
Задание 3. Какие величины совпадают на Плюке и на Земле?
атомная доля водорода в воде
относительная атомная масса кислорода
массовая доля водорода в воде
относительная молекулярная масса серной кислоты
Ответ: Все совпадают
Задание 4. Для создания произведений искусства используют различные химические вещества. Из чего сделаны изображенные ниже скульптуры? Установите правильное соответствие.


Ответ: Памятник А.С. Пушкину, Москва → Cu + Sn Венера Милосская, Лувр, Париж → CaCO3 Малахитовая чаша, Эрмитаж, Санкт-Петербург → (CuOH)2CO3 «Маша и Медведь» → SiO2
Задание 5. Один из самых красивых драгоценных камней – изумруд – описывается формулой
Be₃Al₂Si₆Oₓ.

Представьте состав изумруда в виде комбинации оксидов. Запишите числа a, b, c в формуле aBeO · bAl₂O₃ · cSiO₂. Если встретится единичный коэффициент, его тоже указывайте.

Ответ: 3, 1, 6
Задание 6. Найдите x в формуле Be₃Al₂Si₆Oₓ.
Ответ: 18
Задание 7. Пероксидами называют производные пероксида водорода H₂O₂, в котором атомы водорода замещены на атомы металла в соответствии с их валентностью.
Запишите химическую формулу пероксида бария.
Задание 8. При нагревании смеси магния с пероксидом бария происходит яркая вспышка. Продуктами химической реакции являются два сложных твёрдых вещества. Запишите их химические формулы.
Задание 9. На картинке приведена диаграмма, описывающая состав сухого воздуха в объёмных процентах.
Сделайте выводы из этой диаграммы. Для каждого из приведенных ниже утверждений укажите, верное оно или нет.
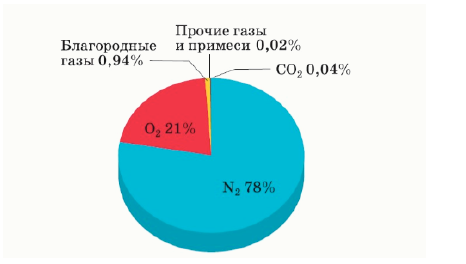
Воздух – это смесь газов.
Воздух почти полностью (больше, чем на 99,9%) состоит из простых веществ.
В составе сухого воздуха совсем нет сложных веществ.
Основной компонент воздуха по объёму – азот.
Основной компонент воздуха по массе – кислород.
99% воздуха – это двухэтажные молекулы.
В составе воздуха не менее 5 веществ.
Задание 10. В каком простом веществе массовая доля водорода наибольшая? Запишите формулу вещества и массовую долю водорода в процентах.
Задание 11. В каком сложном веществе массовая доля водорода наибольшая? Подсказка: при обычных условиях вещество газообразное. Запишите формулу вещества и массовую долю водорода в нём в процентах с точностью до целых.
→ Получить все ответы на олимпиаду
Задание 12. Известно, что крейский реагирует с газообразным азотом в массовом соотношении 3 : 2, при этом образуется единственный продукт – вещество X.
Запишите химическую формулу X.
Задание 13. Вещество X при нагревании в кислороде сгорает, образуя одно простое и одно сложное вещество. Запишите формулы этих веществ.
Простое вещество —
Сложное вещество —
→ Получить все ответы на олимпиаду
Задание 14. При длительном нагревании порошка металла осмия (Δr = 100) в кислороде не остаётся твёрдого остатка, так как оксид осмия летуч. Известно, что в этом оксиде масса осмия почти в три раза больше массы кислорода.
Запишите химическую формулу этого оксида.
Задание 15. Порошок сплава осмия с платиной массой 29,0 г после длительного прокаливания на воздухе стал весить 19,5 г.
Определите массовую долю осмия в сплаве в процентах. Ответ округлите до целого числа.
→ Получить все ответы на олимпиаду
Задание 16. Сколько атомов платины приходится в этом сплаве на один атом осмия? Ответ округлите до целого числа.
Задание 17. Итальянский химик Амедео Авогадро установил, что в равных объемах различных газов при одних и тех же условиях содержится одинаковое число молекул. Из перечисленных ниже газов составьте газовые смеси, плотность которых при одних и тех же условиях может быть равна плотности воздуха. Каждая из составленных вами смесей должна содержать два различных газа. Приведите все возможные пары, удовлетворяющие условию задачи. Например 1 (водород) и 2 (гелий), пара: 12.
1) водород
2) гелий
3) углекислый газ
4) хлор
В каждой паре записывайте цифры в порядке возрастания. Например: 25.
→ Получить все ответы на олимпиаду
Задание 18-19. Колларгол — лекарственное средство, содержащее серебро. Оказывает вяжущее, антисептическое и противовоспалительное действие. Представляет собой зеленовато- или синевато-черные мелкие пластинки с металлическим блеском. Применяется в виде водных растворов.

Для опыта взяли 10 мл 2%-го раствора колларгола и провели с ним следующие эксперименты.
1. Раствор налили в чашку для выпаривания, накрыли листом фильтровальной бумаги для защиты от пыли и оставили на несколько дней до полного испарения воды.
2. Полученные кристаллы прокалили в муфельной печи. В результате прокаливания образовался порошок металла светло-серого цвета.
3. Порошок охладили до комнатной температуры, промыли водой, отфильтровали и высушили.
4. Отмытый и высушенный порошок снова поместили в печь, сильно нагрели. На дне чашки образовались капельки металла.
5. После охлаждения с помощью точных весов измерили массу полученного металла. Она составила 140 мг.
Укажите, какие описанные выше действия относятся к физическим явлениям, а какие — к химическим.
Раствор налили в чашку для выпаривания, накрыли листом фильтровальной бумаги, для защиты от пыли, и оставили на несколько дней до полного испарения воды.
Полученные кристаллы прокалили в муфельной печи. В результате прокаливания образовался порошок металла светло-серого цвета.
Порошок охладили до комнатной температуры, промыли водой, отфильтровали и высушили.
Отмытый и высушенный порошок снова поместили в печь, сильно нагрели. На дне чашки образовались капельки металла.
После охлаждения с помощью точных весов измерили массу полученного металла. Она составила 140 мг.
→ Получить все ответы на олимпиаду
Задание 20. В цилиндре (см. рис. 1) смешали 200 мл кислорода и 100 мл газа X. С помощью электрической искры смесь подожгли (см. рис. 2). Кислород и газ X прореагировали со взрывом без остатка. Продуктами реакции являются только углекислый газ и пары воды. Известно, что X — бинарное соединение, молекулы которого состоят из пяти атомов.
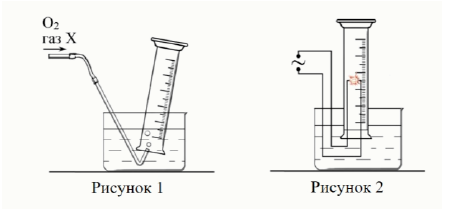
Запишите названия химических элементов, из которых состоит вещество X.
Названия вводите в поля для ответа, используя русскую раскладку клавиатуры, строчными буквами, например: фосфор.
Задание 21. Рассчитайте относительную молекулярную массу газообразного соединения X. Ответ округлите до целых.
→ Получить все ответы на олимпиаду

Олимпиада по химии ответы 9 класс школьный этап 2025
Задание 1. На картине Л.З. Танклевского «Портрет химика Алексея Ивановича Шаврыгина» показано, как учёный измеряет показатель преломления перегоняемой жидкости на рефрактометре. Соотносите названия лабораторной посуды с номерами, которыми она обозначена на рисунке.


Ответ: 1 — аппарат киппа 2 — колба Вюрца 3 — эксикатор 4 — прямой холодильник 5 — колба-приемник
Задание 2-5. Имеются 4 навески порошков металлов, все навески имеют одинаковую массу. Металлы – железо, цинк, алюминий, магний. Металлы сожгли в избытке кислорода и взвесили продукты сгорания. Запишите формулы продуктов сгорания и расположите их в порядке возрастания массы.
Продукт 1 (наименьшая масса)
Продукт 2
Продукт 3
Продукт 4 (наибольшая масса)
Ответ: 2) MgO 3) ZnO 4) Al2O3 5) Fe2O3
Задание 6-7. В аппарат Киппа (на рис. показан цифрой 1) поместили кусочки мрамора и залили соляную кислоту. Выделился газ X, который пропустили в цилиндр с дистиллированной водой (на рисунке показан цифрой 2).
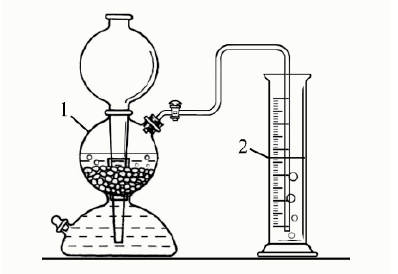
После пропускания газообразного вещества X масса цилиндра с водой увеличилась на 1,1 г.
В цилиндр с раствором X добавили избыток известковой воды, наблюдали выпадение осадка белого цвета.
Какой газ X получали в аппарате Киппа? Приведите его химическую формулу.
Ответ: CO2
Какова масса осадка, выпавшего после добавления избытка известковой воды к раствору газа X? Ответ выразите в граммах и округлите до десятых.
Ответ: 2.5
Задание 8. Выберите вещества, действуя на которые соляной кислотой, можно количественно получить хлорид цинка.
ZnO
Zn(NO₃)₂
Zn₂(OH)₂CO₃
ZnSO₄
Na₂ZnO₂
ZnBr₂
→ Получить все ответы на олимпиаду
Задание 9. Даны смеси газов (в неизвестных соотношениях). Как изменится средняя молярная масса каждой смеси при протекании реакции между газами? Установите правильное соответствие.

Задание 10-11. Навеска металла массой 2,00 г полностью растворяется в избытке соляной кислоты с выделением газа, объём которого составляет 377 мл (в пересчёте на н.у.).
Определите металл, в ответе укажите его символ. Предложите два разных решения.
Металл 1 (с меньшей атомной массой) –
Металл 2 (с бóльшей атомной массой) –
→ Получить все ответы на олимпиаду
Рассчитайте массу продукта реакции соляной кислоты с более тяжёлым металлом. Ответ приведите в граммах, с точностью до десятых.
Задание 12-13. Вещество ионного строения состоит из двух элементов. Положительный и отрицательный ионы имеют одинаковую электронную конфигурацию. При взаимодействии вещества с водой выделяется газ, в молекуле которого столько же электронов, сколько в каждом из ионов по отдельности.
Определите неизвестные вещества и ионы, приведите их формулы. В формуле иона заряд указывайте после символа элемента.
Сколько электронов содержится в молекуле газа?
→ Получить все ответы на олимпиаду
Задание 14. Химические связи бывают разные — короткие и длинные. Даны некоторые ковалентные связи и их длины (в относительных единицах). Каждой связи поставьте в соответствие правильную длину.
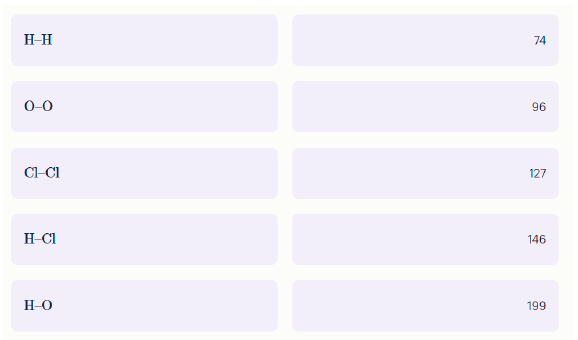
Задание 15-16. Белый фосфор состоит из молекул P₄. В отличие от других видов фосфора, он растворим в сероуглероде CS₂. При полном сжигании образца такого раствора получили 7,10 г белого порошка и 43,68 л (н.у.) смеси газов.
Определите массу раствора (в г). Ответ приведите с точностью до десятых.
Определите массовую долю белого фосфора (в %) в этом растворе. Ответ приведите с точностью до десятых.
→ Получить все ответы на олимпиаду
Задание 17-18. Коричневый порошок X, используемый в качестве катализатора при получении кислорода в лаборатории, при прокаливании разлагается так, что масса твердого остатка Y оказывается на 18,4 % меньше массы X. Вещество Y при выдерживании в кислороде переходит в вещество Z, содержащее 28,0 % кислорода по массе.
Установите вещества X, Y, Z, приведите их формулы.

Укажите все правильные степени окисления атомов металла в Z.
Задание 19-20. Вещество XY – бинарное соединение светло-желтого цвета. Его можно получить реакцией обмена между растворами двух электролитов (см. фото).
Этой реакции соответствует краткое ионное уравнение:
X⁺ + Y⁻ = XY
Соотношение масс ионов X⁺ и Y⁻ в данной реакции составляет
m(X⁺)/m(Y⁻) = 1/1.176
Элементы X и Y находятся в одном периоде Периодической системы химических элементов Д.И. Менделеева.
Определите элементы X и Y. В ответ введите их символы.
→ Получить все ответы на олимпиаду
Вещество XY не растворяется ни в воде, ни в органических растворителях. При нагревании плавится с разложением. Под действием света разлагается. Кристаллическая структура XY похожа на гексагональную структуру кристаллов льда, поэтому введение небольшого количества аэрозоля в виде микроскопических кристалликов XY в дождевое облако вызывает в нём конденсацию водяного пара.
Проанализируйте описанные выше свойства соединения XY, укажите области его применения.

Задание 21-22. Дана схема окислительно-восстановительной реакции.
X + Cl₂ + H₂O ⟶ H₃PO₄ + Br₂ + Y
Определите вещества X и Y, приведите их формулы.
Найдите коэффициент перед формулой H₂O в уравнении реакции, если минимальный коэффициент в уравнении равен 2.
→ Получить все ответы на олимпиаду

Олимпиада по химии ответы 10 класс школьный этап 2025
Задание 1. В 1 моль вещества ионного строения содержится суммарно 3 моль ионов. Катионы и анионы имеют одинаковую электронную конфигурацию. Массовая доля катионов составляет 36,0 %. Определите вещество, приведите его формулу.
Ответ: CaCl2
Задание 2-4. При сжигании 0,1 моль простого вещества молекулярного строения образовалось 0,1 моль оксида Y, массовая доля кислорода в котором равна 43,6 %. Плотность паров этого вещества по воздуху равна 7,6.
Установите молекулярные формулы простого вещества и образующегося оксида.
Простое вещество –
Оксид –
Сколько валентных электронов содержит атом элемента, образующего простое вещество?
Укажите пространственное строение молекулы простого вещества.
квадрат
октаэдр
треугольник
тетраэдр
правильный шестиугольник
куб
шар
Ответ: 2) Простое в-во: Р4 Оксид: P4O6 3) 20 4) тетраэдр
Задание 5-7. При электролизе водного раствора натриевой соли одноосновной предельной карбоновой кислоты с неразветвлённым скелетом на аноде образовались газ и жидкость, массовая доля углерода в которой составляет 83,7 %. Установите формулы исходной соли, жидкости и газообразного продукта сплавления твёрдой соли с избытком гидроксида натрия.
Пример записи формулы соли: C40H8ICOONa.
Запишите формулу исходной соли.
Запишите формулу жидкости.
Запишите формулу газообразного продукта сплавления.
Ответ: 5) C3H7COONa 6) C6H12 7) C3H8
Задание 8-10. Соединение с молекулярной формулой C₄H₅Br₂ не имеет оптических изомеров, а при нагревании со спиртовым раствором щелочи образует единственный органический продукт — вещество состава C₄H₆, которое легко полимеризуется. Установите структуры упомянутых в условии веществ и ответьте на вопросы.
Укажите номера атомов углерода в названии исходного соединения, с которыми соединены атомы брома.
Сколько двойных связей содержит продукт C₄H₆? В поле ответа введите число, если двойных связей нет, введите 0.
Сколько двойных связей содержит элементарное звено полимера, который получается из C₄H₆? В поле ответа введите число, если двойных связей нет, введите 0.
→ Получить все ответы на олимпиаду
Задание 11. Одним из способов определения влаги в строительных образцах является карбидный метод. Исследуемый образец, ампулу с карбидом кальция (CaC₂) и несколько металлических шариков помещают в прочный стальной сосуд. Сосуд закрывают крышкой, в которую вмонтирован манометр. Давление в сосуде приводят к атмосферному. После встряхивания сосуда металлические шарики разбивают стеклянную ампулу и карбид кальция начинает реагировать с влагой в образце.
Какой газ выделяется в ходе реакции? В ответ запишите формулу этого газа.
50 г исследуемого образца плотностью 2 г/см³, ампулу карбида кальция объёмом 15 см³ и металлические шарики общим объёмом 3,5 см³ поместили в сосуд объёмом 700 см³. Считайте, что эти объёмы не меняются в ходе эксперимента. Сосуд закрыли, привели давление внутри сосуда к атмосферному и затем встряхнули. После окончания реакции давление в сосуда увеличилось настолько, что молярный объём газа по окончании измерения стал равен 8,15 л/моль.
Рассчитайте массовую долю воды (%) в исследуемом образце. В ответ запишите число, округлив его до десятых.
→ Получить все ответы на олимпиаду
Задание 12-14. Одним из источников энергии на космических станциях может служить реакция α-распада плутония-238. Изотоп какого элемента (помимо α-частицы) образуется в ходе данной
реакции?
Запишите массовое число изотопа этого элемента.
В результате распада 1 моль плутония-238 выделяется 6,4·10⁸ кДж энергии. Рассчитайте массу (в т) авиационного бензина с удельной теплотой сгорания 44,1 МДж/кг, который необходимо сжечь, чтобы выделилось такое же количество энергии. Ответ округлите до десятых.
→ Получить все ответы на олимпиаду
Задание 15. Для расчета массы металла, который выделяется на катоде в процессе электролиза, используют закон Фарадея:
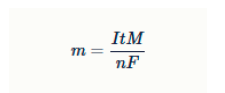
m = (ItM)/(nF)
где m — масса выделившегося металла, г I — сила тока, А t — время проведения электролиза, с
M — молярная масса металла, г/моль F ≈ 96500 Кл/моль — постоянная Фарадея n — количество электронов, участвующих в восстановлении иона металла до металла.
В раствор соли нитрата одновалентного металла опустили электроды и начали пропускать ток силой 8 А в течение 1 часа, при этом выделилось 14,5 г металла. Определите металл, если выход реакции составил 45 %, а электролиз проводили до тех пор, пока не прекратилось выделение металла. В ответ запишите символ металла.
→ Получить все ответы на олимпиаду
Задание 16. Дана схема превращений, в которой все вещества содержат один и тот же элемент Э, а X – простое вещество:

X →(Mg) X₁ →(H₂SO₄) X₂ →(HI, AlI₃ (кат.)) X₃ →(Na(Hg)) X₄
X₁ содержит 36,8 % элемента Э по массе, а X₃ – 17,7 % этого элемента.
Определите вещества X, X₁ – X₄, если превращение X₃ → X₄ похоже на то, которое вы уже изучали в теме «Алканы». В ответ запишите молярные массы (г/моль) этих веществ с точностью до целых.
→ Получить все ответы на олимпиаду
Задание 17. Из углеводорода A, который в 1,5 раза тяжелее неона, в несколько стадий получили углеводород G, который почти в 2 раза тяжелее A:
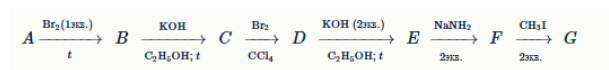
A →[Br₂ (1 экв), t] B →[KOH, C₂H₅OH; t] C →[H₂ (кат.), 2 экв] D →[KOH (2 экв), C₂H₅OH; t] E →[NaNH₂, 2 экв] F →[CH₃I, 2 экв] G
Известно, что амид натрия NaNH₂ проявляет очень сильные основные свойства, а связь водорода с углеродом при связи C≡C обладает повышенной (по сравнению со связями C-H в алканах) кислотностью.
Определите неизвестные вещества. В ответе приведите их молярные массы (г/моль, с точностью до целых).
→ Получить все ответы на олимпиаду
Задание 18-22. Имеются растворы трёх солей – A, B, C. Все три раствора – бесцветные, окрашивают пламя в жёлтый цвет. Раствор бинарного вещества A может реагировать с раствором нитрата свинца, давая чёрный осадок. Раствор вещества B обесцвечивает подкисленный раствор перманганата калия. Растворы веществ A и B смешали, а затем к порции полученной смеси добавили разбавленную соляную кислоту, при этом образовался осадок простого вещества X. Такое же вещество X выпадает в осадок, если добавить разбавленную бромоводородную кислоту к раствору вещества C. Также известно, что:
- вещество C раньше использовалось в фотографии в качестве закрепителя;
- вещества B и C содержат атомы одних и тех же химических элементов;
- в составе ангидрида вещества B масса кислорода больше массы второго элемента в 1,5 раза, а в составе ангидрида вещества C масса кислорода составляет 75 % от массы второго элемента.
Определите вещества A, B, C, X. В ответе приведите их формулы.
Найдите сумму минимальных целочисленных коэффициентов в уравнении реакции сернокислого раствора перманганата калия с раствором вещества B.
→ Получить все ответы на олимпиаду
Задание 23. С несколькими газами провели один и тот же эксперимент. Цилиндр наполняли смесью газа с избытком кислорода (рис. 1). С помощью электрической искры смесь поджигали (рис. 2). Неизвестный газ полностью сгорал в кислороде, продуктами реакции являлись только оксид углерода (IV) и пары воды.
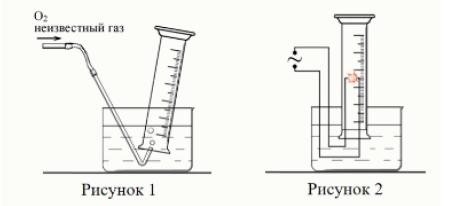
Все газы, с которыми проводили этот опыт, являются бинарными соединениями. Вещества A и D – гомологи. Некоторые сведения о результатах экспериментов и составе неизвестных газов приведены в таблице ниже.
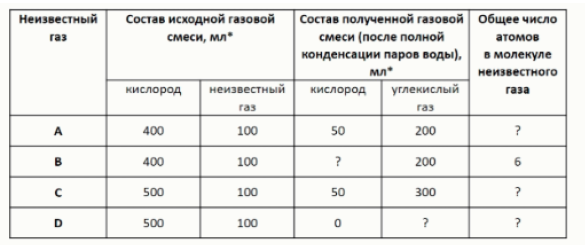
Объёмы газов измерены при одинаковых условиях (давлении и температуре).
Установите состав газов A-D. В поля для ответов введите значения их молярных масс в г/моль, округлив до целых.
→ Получить все ответы на олимпиаду
Задание 24-26. В Крыму, в г. Красноперекопск, находится промышленное предприятие, которое специализируется на выпуске химической продукции. Главным образом получают вещества, образованные элементом X.
Сначала воду из солёных озёр, находящихся рядом с Красноперекопском, перекачивают в испарительные бассейны. Вода постепенно испаряется, концентрация солей в растворе возрастает. В специальных колоннах полученный рассол обрабатывают веществом Y₂, протекает реакция:
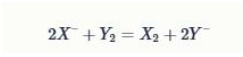
2X⁻ + Y₂ = X₂ + 2Y⁻
Образующееся простое вещество X₂ выделяют из раствора отгонкой с паром или выдуванием воздухом (воздушно-десорбционный способ).
Определите элементы X и Y, если известно, что они находятся в одной подгруппе Периодической системы химических элементов Д.И. Менделеева. В ответ введите символы элементов.
Из рассола озера Старое методом дробной перекристаллизации можно получить кристаллогидрат, состав которого Me₂X₂ · 6H₂O (Me – некоторый металл). Массовая доля ионов X⁻ в кристаллогидрате составляет 54,8 %.
→ Получить все ответы на олимпиаду
Определите металл Me. Введите его символ в поле для ответа.
Одним из органических веществ, выпускаемых заводом в Красноперекопске, является продукт присоединения вещества X₂ к простейшему алкину. Определите общее число атомов в молекуле данного продукта.
→ Получить все ответы на олимпиаду

Олимпиада по химии ответы 11 класс школьный этап 2025
Задание 1-3. Бесцветное кристаллическое вещество массой 6,00 г сожгли в кислороде, получив при этом 4,40 г углекислого газа, 2,24 л (н.у.) азота и 3,60 г воды. А при нагревании 6,00 г этого вещества с избытком раствора гидроксида калия выделяется 4,48 л (н.у.) аммиака.
Установите молекулярную формулу вещества (в формате CхHyNzOa, единичный индекс не записывается).
Запишите тривиальное название вещества.
Найдите сумму минимальных целочисленных коэффициентов в реакции вещества с гидроксидом калия.
Ответ: CH4N2O, мочевина, 6
Задание 4-5. Вещества А и Б ионного строения имеют одинаковые молярные массы, а 1 моль каждого вещества содержит суммарно 3 моль ионов. Все ионы в обоих веществах имеют одинаковую электронную конфигурацию. Массовая доля катионов в веществе А равна 74,2 %, массовая доля катионов в веществе Б составляет 38,7 %.
Определите вещества А и Б. В ответе запишите их формулы.
Запишите молярную массу этих веществ (в г/моль, с точностью до целых).
Ответ: Вещество А – Na2O Вещество Б – MgF2 , 62 ,
Задание 6-8. Простые вещества X и Y, соответствующие элементам-неметаллам одной группы, имеют атомное строение и одинаковую кристаллическую структуру. В этих кристаллах все атомы четырёхвалентны, а все связи – одинарные. Первое вещество растворяется в концентрированной азотной кислоте, но не реагирует с концентрированной щелочью, а второе – наоборот.
Запишите формулы простых веществ X и Y.
Сколько молей химических связей содержится в 42 г X? Ответ – натуральное число.
Сколько молей химических связей содержится в 42 г Y? Ответ – натуральное число.
Ответ: Вещество X X: C, Вещество Y Y: Si, X: 7, Y: 3
Задание 9-11. Дана схема превращений:
CₙH₂ₘOₙ → X → C₃H₈O → Y → C₃H₅O₂Cl → Z → CₘH₂ₘOₘ
Известно, что m = 3n, а вещество Z содержит азот. Расшифруйте схему.
Найдите значения m и n.
m = Число
n = Число
Приведите молекулярную формулу вещества Z (в формате CxHyNzOa, единичный индекс не записывается).
Напишите формулу реагента, который используется на последней стадии.
→ Получить все ответы на олимпиаду
Задание 12. В пяти пронумерованных пробирках находятся твёрдые белые порошки нерастворимых в воде веществ. Чтобы определить содержимое пробирок, с ними провели ряд экспериментов, результаты которых представлены в виде таблицы:
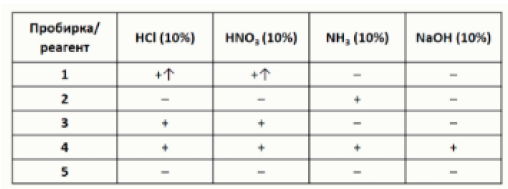
– растворение
– – отсутствие видимых изменений
↑ – выделение газа
→ Получить все ответы на олимпиаду
Определите содержимое пробирок, установив соответствие между номером пробирки и формулой вещества.

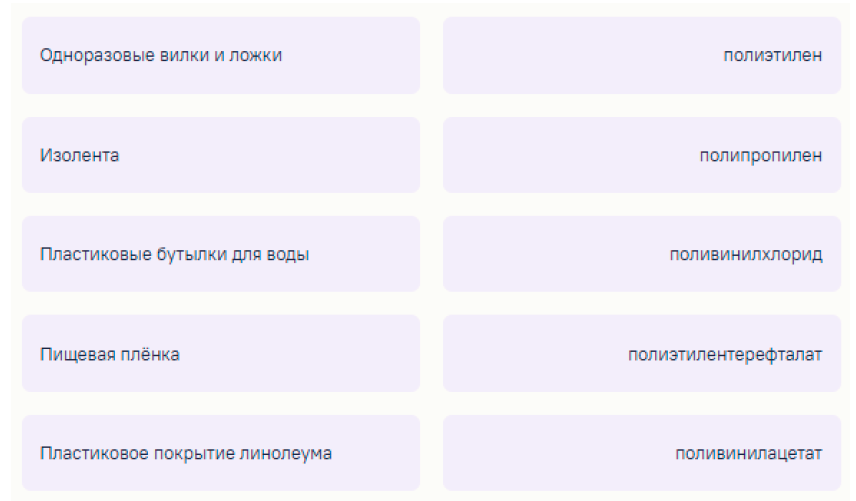
Задание 13. Установите соответствие между предметом и полимером, из которого его изготавливают.
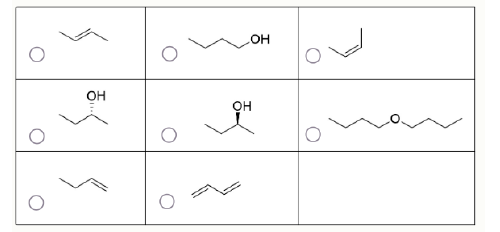
Задание 14-18. Часто в ходе химических реакций с органическими соединениями помимо основного продукта образуется много других. Для каждой реакции выберите ВСЕ вещества, которые могут являться её продуктами (не обязательно главными).
→ Получить все ответы на олимпиаду
Выберите ВСЕ вещества, которые могут являться продуктами реакции (не обязательно главными).
Задание 19. Иодометрия – это важный титриметрический метод определения концентраций
окислителей. Для проведения данного анализа к алквоте раствора окислителя добавляют
избыток раствора иодида калия, после чего выделившийся в ходе окислительно-
восстановительной реакции иод титруют стандартным раствором тиосульфата натрия. Для
иодометрического определения взяли одинаковые алквоты 2,00 % водных растворов:
- перманганата калия;
- дихромата аммония;
- бромата натрия;
- пероксида водорода.
Расположите растворы окислителей в порядке уменьшения (от наибольшего к
наименьшему) объёма раствора тиосульфата натрия, который пойдёт на титрование иода,
выделившегося при взаимодействии их алквот с подкисленным раствором иодида калия.
Плотности всех растворов примите равными 1 г/см³.
→ Получить все ответы на олимпиаду

Задание 20-23. В ходе лабораторной работы по химии в 10 классе при изучении курса органической химии учитель Колбочкин предложил учащимся взять высококалорийный пищевой продукт X (который можно легко купить в продуктовых магазинах или фермерских лавках) и нагреть его вместе с концентрированным раствором гидроксида натрия. При этом образуются смесь органических веществ одного класса и органическое вещество Z. Компонент смеси Y содержит 18 атомов углерода. Продукт взаимодействия вещества Y с соляной кислотой не реагирует с бромной водой. Вещество Y способствует умягчению жёсткой воды. Вещество Z используется в косметологии, при его нагревании с кристаллическим гидросульфатом калия образуется органическое вещество Q (массовая доля углерода 64,3 %, массовая доля водорода 7,1 %), которое может присоединять бром и реагировать с реактивом Толленса (аммиачным раствором оксида серебра) с образованием осадка простого вещества.
Как называется пищевой продукт X? В ответ запишите одно слово.
Какова среда водного раствора вещества Y?
Чему равна молярная масса вещества Z? Дайте ответ в г/моль с точностью до целых.
Назовите вещество Q по правилам ИЮПАК.
→ Получить все ответы на олимпиаду
Задание 24-27. Вещество X может растворяться в ацетоне (рис. 1). При добавлении нескольких капель воды окраска раствора меняется (рис. 2). Небольшое количество полученного раствора кисточкой нанесли на фильтровальную бумагу (рис. 3) и полученную бумагу с «невидимой» надписью нагрели на плитке (рис. 4). Таким способом раньше писали зашифрованные послания.

Также известно, что:
- При добавлении к водному раствору, содержащему 0,01 моль X, избытка раствора нитрата серебра выпадает белый творожистый осадок массой 2,87 г.
- При длительном прокаливании образца X количеством вещества 0,01 моль потеря массы составляет 1,08 г, а пары летучего вещества полностью поглощаются фосфорным ангидридом.
- Массовая доля металла, входящего в состав X, в его оксиде составляет 78,7 %. Валентность металла в оксиде — такая же, как в веществе X.
При расчётах необходимо округлять атомные массы элементов до целых значений, кроме хлора, для него примите атомную массу 35,5.
→ Получить все ответы на олимпиаду
Чему равна валентность металла в X? Ответ необходимо указать арабской цифрой, например, 1.
Как называется металл, входящий в состав X? Приведите русское название.
Чему равна молярная масса X? Ответ приведите в г/моль с точностью до целых.
Как по-другому называются «невидимые» чернила? Приведите только прилагательное во множественном числе, например: чистые.
→ Получить все ответы на олимпиаду
Задание 28-29. В 1839 году после многолетней серии опытов французский художник Луи Дагер представил процесс получения дагерротипа членам Французской академии наук. Так началась история фотографии.
Суть дагерротипии состояла в следующем: на пластинку металла X золотисто-розового цвета наносили слой металла Y, полируя его до зеркального блеска. Затем в темноте обрабатывали парами простого вещества, неметалла Z₂ (состоит из двухэтомных молекул).
Пары Z₂ имеют красивую фиолетовую окраску. В результате реакции на поверхности пластинки образовывался тончайший слой светочувствительного соединения YZ.
→ Получить все ответы на олимпиаду
Затем пластинку помещали в камеру-обскуру (прообраз фотокамеры) и открывали объектив на 15–30 минут. Под действием света в светочувствительном слое соединение YZ разлагалось, возникало скрытое изображение. Чтобы его проявить, пластинка обрабатывалась парами металла Q, который является жидкостью при обычных условиях. В результате взаимодействия металлов Y и Q на засвеченных участках образовывался сплав, рассеивающий отражённый от него свет. После этого изображение закреплялось путём промывания в растворе тиосульфата натрия. Соединение YZ на незасвеченных участках превращалось в растворимое комплексное соединение и переходило в раствор.
Определите элементы X, Y, Z, Q. Известно, что металлы X и Y находятся в одной подгруппе Периодической системы химических элементов Д.И. Менделеева. Элементы Y и Z – в одном периоде. Введите символы химических элементов X, Y, Z, Q в поля для ответа.
При взаимодействии соединения YZ с раствором тиосульфата натрия образуется комплексный анион с зарядом 3. Рассчитайте молярную массу данного аниона, выразите её в г/моль и округлите до целых.
→ Получить все ответы на олимпиаду
Задание 30-32. Выброс нуклида ¹³⁷X в окружающую среду происходит в основном в результате ядерных испытаний и аварий на предприятиях атомной энергетики. Это – один из главных компонентов радиоактивного загрязнения биосферы. ¹³⁷X претерпевает бета-распад:
¹³⁷X → ¹³⁷Ba + ε
Период полураспада около 30 лет.
Определите элемент X. Введите его символ в поле для ответа.
→ Получить все ответы на олимпиаду
В 1986 году во время аварии на Чернобыльской атомной электростанции (ЧАЭС) из разрушенного реактора было выброшено большое количество радионуклидов, в том числе и ¹³⁷X. В каком году его активность снизится в 4 раза по сравнению с первоначальной?
¹³⁷X является дочерним продуктом β-распада радиоактивного нуклида некоторого элемента. Определите этот элемент. Введите его символ в поле для ответа.




